

为深入贯彻党的二十届三中全会精神,落实《国务院办公厅关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》(国办发〔2024〕53号)要求,进一步优化创新审查和优先审批工作,加强申请人和审查专家的沟通,强化对创新医疗器械和优先审批医疗器械研发和注册的技术指导,引导申请人开展满足临床需求的创新医疗器械设计开发,根据《国家药监局关于发布创新医疗器械特别审查程序的公告》(2018年第83号)《食品药品监管总局关于发布医疗器械优先审批程序的公告》(2016年第168号),器审中心制定了《医疗器械技术审评中心创新医疗器械特别审查申请审查实施细则》《医疗器械技术审评中心医疗器械优先审批申请审核实施细则》,现予发布。
特此通告。
附件:
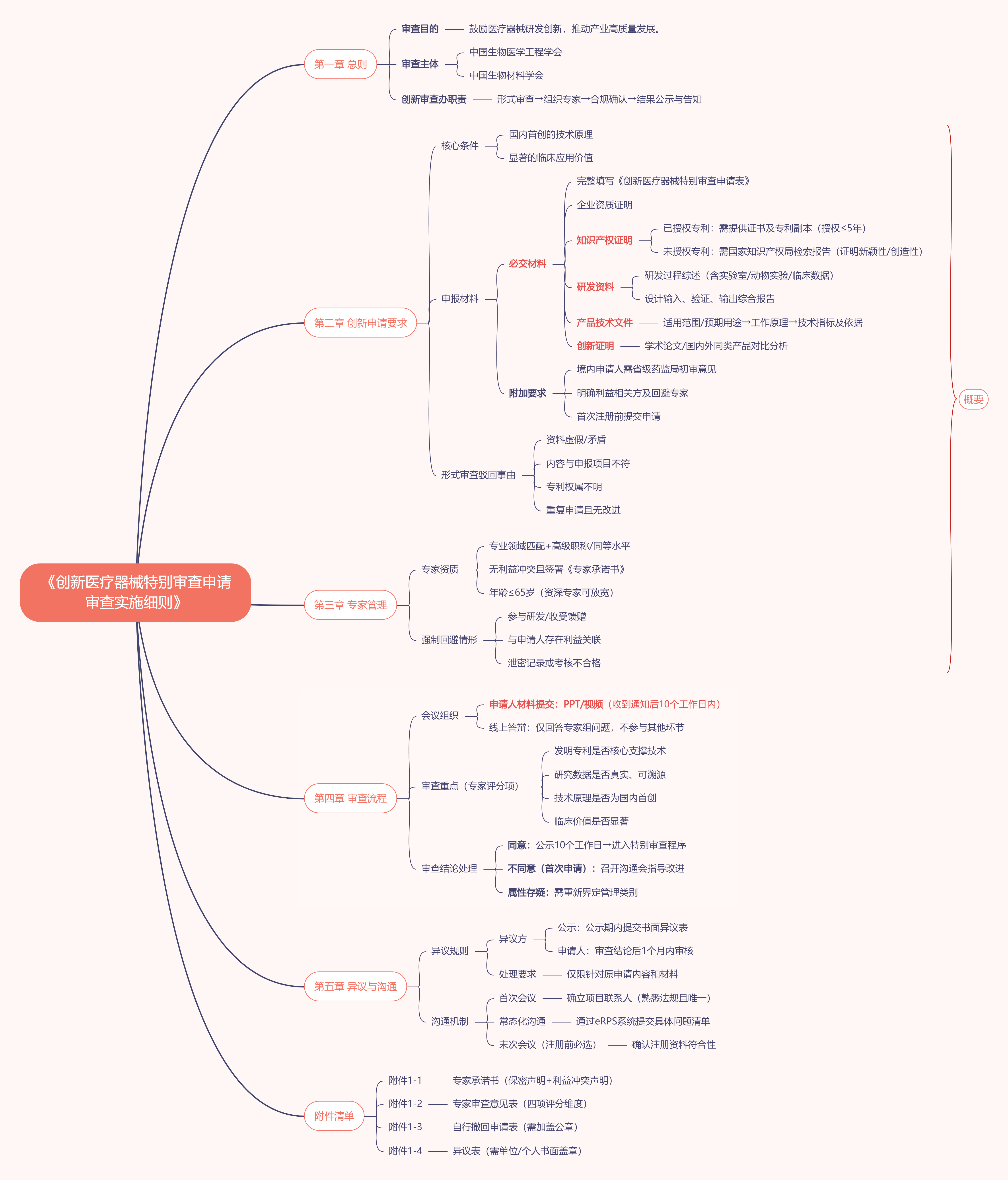
1.医疗器械技术审评中心创新医疗器械特别审查申请审查实施细则(下载)
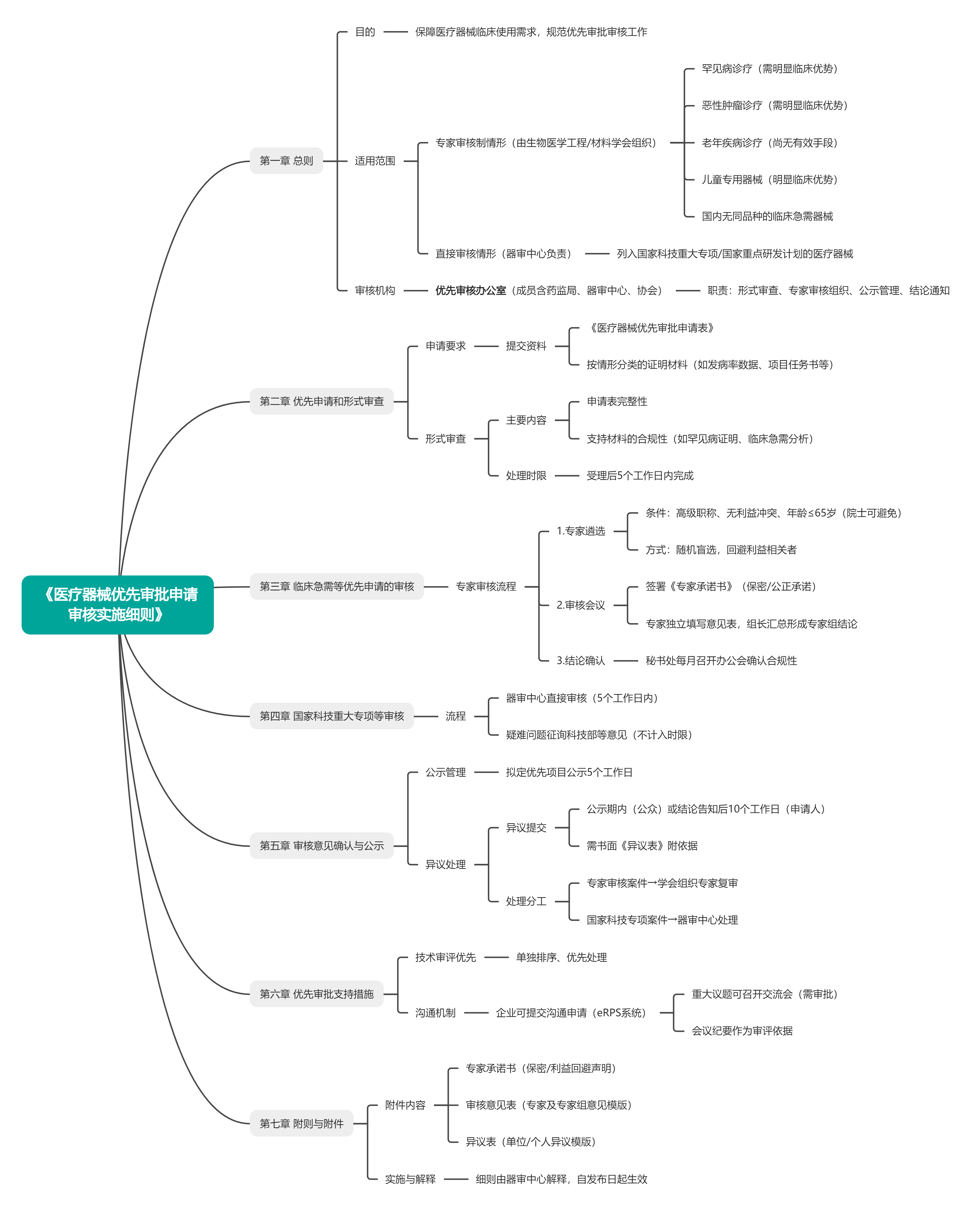
2.医疗器械技术审评中心医疗器械优先审批申请审核实施细则(下载)
国家药品监督管理局
医疗器械技术审评中心
2025年4月17日

小编带您划重点,【思维导图】让你读懂政策核心变化,快来高速学习吧~
Copyright ?2020 北京帝康医药投资管理有限公司 版权所有
京ICP备20001702号-1 ![]() 京公网安备 11011502006138号 互联网药品信息服务资格证编号:(京)网药械信息备字(2025)第 00212 号
京公网安备 11011502006138号 互联网药品信息服务资格证编号:(京)网药械信息备字(2025)第 00212 号